企业名称:重庆一可环保工程有限公司
行政电话:023-68186413
市场经理:18680862016
邮箱:ecoepe@163.com
网址:www.ecoepe.com
公司地址:重庆市九龙坡区科园二路137号申基会展国际B栋19楼
物理、化学和生物法是当前普遍使用的传统废水处理技术。它们主要应用于成分较简单、生物降解性较好、浓度较低的废水处理。但当废水中含有难降解有机物或生物毒性污染物时,利用传统废水处理技术降解废水面临着极大挑战,高级氧化技术便应运而生。
高级氧化技术是一种基于化学氧化法的新技术,是20世纪80年代开始形成的处理有毒有害污染物的技术,它的特点是反应能够产生大量羟基自由基,该自由基具有极强的氧化性,是广谱氧化剂,几乎可以与水中任何物质发生反应,能够将有机污染物有效地分解,甚至彻底转化为无害有机物,如CO2和H2O等。
一般羟基自由基与有机物的反应可归纳为以下三种类型:
(1)脱氢反应
RH+·OH→H2O+·R→进一步氧化
(2)亲电加成
PHX+·OH→·HOPHXR
(3)电子转移
RX+·OH→·RH++OH-
通过上述反应,有机物反应形成活化的有机自由基,使其更容易氧化成其它有机物或产生自由基联锁反应,从而使有机物迅速降解。
高级氧化技术通常包括以下工艺:湿式空气氧化法(WAO)和湿式催化氧化法(CWAO),超临界水氧化(SCWO)及超临界催化氧化(CSCWO),光化学氧化及光催化氧化(如O3/UV、H2O2/UV、O3/H2O2/UV、UV/O2/H2O2和UV/TiO2等),声化学氧化法(如US(超声波)/UV、US/UV/H2O2、US/UV/TiO2、US/UV/O3、US/UV/Fe2+、US/电解、US/O3、US/H2O2、US/Fe2+和UV/TiO2等)芬顿试剂及类芬顿试剂法(如H2O2/Fe2+、H2O2/Fe3+、UV/Fe2+/H2O2、H2O2/Fe2+(Fe3+)/UV、Fe2+/O2/H2O2、H2O2/Fe2+-草酸和Fe2+/UV/O2/H2O2等),组合臭氧氧化法,高能辐射工艺和高压脉冲放电技术等。
其中,电化学水处理技术具有适应性广、操作简便灵活、无需添加氧化还原剂、对环境友好等优点,因此具有良好的应用前景。电化学水处理技术就是利用外加电场作用,在特定的电化学反应器内,通过一系列设计的化学反应、电化学过程或物理过程,达到预期的去除废水中污染物或回收有用物质的目的。根据电极反应发生方式的不同,电化学可分为铁炭内电解、电絮凝、电解浮选、电催化氧化。
电催化氧化(Electro-Catalytic Oxidation,ECO)作为高级氧化形式的一种,它是通过阳极反应直接降解有机物,或通过阳极反应产生HO·、O3一类的氧化剂间接降解有机物,这种降解途径使有机物分解更加彻底,不易产生有毒害作用的中间产物,更符合环境保护要求。
电催化氧化基本原理是使有机污染物直接在电极上得失电子而发生氧化还原转变,或利用在电极反应产生的各种强氧化剂使污染物被降解。
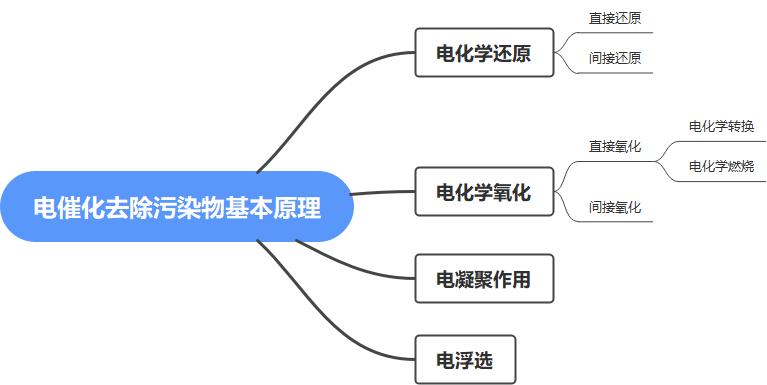
图2-1 电催化去除污染物基本原理
(1)直接还原:污染物直接在阴极上得到电子而发生还原。
基本反应式为:M2+ + 2e- → M。
许多金属的回收即属于直接还原过程,同时该法可使多种含氯有机物转变成低毒性物质,提高产物的可生物降解性。
如: R-Cl + H+ + 2e- → R-H + Cl- 。
(2)间接还原:利用电化学过程中生成的一些还原性物质如钛Ti3+,钒V2+和铬Cr2+将污染物还原去除,如二氧化硫的间接电化学还原可转化成单质硫:
SO2 + 4Cr2+ + 4H+ → S + 4Cr3+ + 2H2O
(1)直接氧化:污染物直接在阳极失去电子而发生氧化,有机物的直接电催化氧化分两类进行。
A、电化学转换——即把有毒物质转变为无毒物质,或把难生化的有机物转化为易生化的物质(如芳香物开环氧化为脂肪酸),以便进一步实施生物处理;
B、电化学燃烧——即直接将有机物深度氧化为CO2。
有研究表明,有机物在金属氧化物阳极上的氧化反应机理和产物同阳极金属氧化物的价态和表面上的氧化物种有关。
阳极表面氧化过程分两阶段进行:
首先溶液中的H2O或·OH在阳极上形成吸附的氢氧自由基:
MOx + H2O → MOx (·OH) + H+ + e-
然后吸附的氢氧自由基中的氧转移给金属氧化物晶格,形成高价氧化物:
MOx (·OH) → MOx+1 + H+ + e-
当溶液中不存在有机物时,两种状态的活性氧发生氧析出反应:
MOx (·OH) →O2 + MOx + H+ + e-
MOx+1 → MOx + O2
当溶液中存在可氧化的有机物R时,反应如下:
R + MOx (·OH) → CO2 + MOx + H+ + e-
R + MOx+1 → MOx + RO
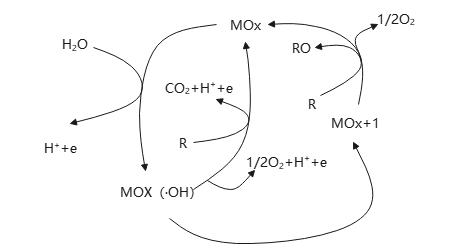
图2-2 氧化物阳极催化氧化处理有机物的过程图
(2)间接氧化
通过阳极反应生成具有强氧化作用的中间产物或发生阳极反应之外的中间反应生成的中间物质(羟基自由基·OH、氧自由基·O2、过氧化羟基自由基·HO2等自由基),氧化被处理污染物,最终达到氧化降解污染物的目的。
为了得到高的转化效率,电催化氧化还原作用过程必须满足以下要求:
(1)氧化还原剂的生成电位必须不靠近析氢或析氧反应的电位;
(2)氧化还原剂的产生速度足够大;
(3)氧化还原剂与污染物的反应速度比其他竞争反应的大;
(4)其他物质(或污染物)在电极上的吸附小。
在电解过程当中,如果采用铝质或铁质的可溶性阳极,通以直流电后,阳极材料会在电解过程当中发生溶解,形成金属阳离子Fe3+、Al3+等,与溶液中的粒子形成具有絮凝作用的胶体物质,这些物质可促使水中的胶态杂质絮凝沉淀,从而实现污染物的去出。
在对废水进行电化学处理过程中,通过电极反应在阴极和阳极上分别析出H2和O2,产生直径很小(约8~15μm)、分散度很高的气泡,作为载体吸附系统中的胶体微粒及悬浮固体上浮,在水面形成泡漠层,用机械方法加以去除,从而达到分离污染物的目的。
可通过调节电流、电极材料、pH值和温度可改变产气量及气泡大小,满足不同需要。
电极——指与电解质接触的电子导体或半导体,它既是电子贮存器,能够实现电能的输入或输出,又是电化学反应发生的场所。
催化电极——首先应该是一个电子导体,其次要兼具催化功能,即:既能导电,又能对反应物进行活化,提高电子的转移速率,对电化学反应进行某种促进和选择。
(1)催化电极的种类
主要分为两大类:二维电极;三维电极;
A. 二维电催化电极
应用最广泛的是钛基氧化物涂层电极(DSA类电极)。
DSA电极——以特殊工艺在金属基体(如Ti钛,Zr锆,Ta钽,Nb铌等)上沉积一层微米或亚微米级的金属氧化物薄膜(如二氧化锡SnO2, 二氧化铱IrO2,二氧化钌RuO2,二氧化铅PbO2等)而制备的稳定电极。DSA类电极通过改进材料及涂层结构提供了较高的析氧过电位,防止阳极氧气的析出,提高其电流效率。
优点:由于DSA类电极的化学和电化学性质能够随着氧化物膜的材料组成和制备方法而改变,因而能够获得良好的稳定性和催化活性。
缺点:有效电极面积很小,传质差,导致单位时空处理效率较低。
B. 三维电催化电极
定义:在原有的二维电极之间装填粒状或其他屑状工作电极材料,致使装填电极表面带电,在工作电极材料表面发生电化学反应。
优点:面积比较大且能以较低的电流密度提供较大的电流强度;粒子之间间距小,物质传质极大改善;单位时空产率和电流效率均极大提高,尤其对低电导率废水,其优势更是明显。
(2)电极材料的种类
A. 金属电极
金属电极是指以金属作为电极反应界面的裸露电极,除碱金属和碱土金属外,大多数金属作为电化学电极均有很多研究报道。
B. 碳素电极
由元素碳组成的电极的总称。可分为天然石墨电极、人造石墨电极、碳电极以及特种碳素电极等四类。
C. 金属氧化物电极
导电金属氧化物电极具有重要的电催化特性,这类电极大多为半导体材料。
D. 非金属化合物电极
一般所说的非金属电极是指硼化物、碳化物、氮化物、硅化物、氯化物等。非金属材料作为电极材料,最大的优势在于这类材料的特殊物理性质,如高熔点、高硬度、高耐磨性、良好的耐腐蚀性以及类似金属的性质等。
电极在电化学处理技术中处于“心脏”的地位,电极的电催化特性是电催化技术的核心内容,即希望电极对目标有机物表现出高的反应速率,并且有好的选择性。
催化电极的功能:既能导电,又能对反应物进行活化,提高电子的转移速率,对电化学反应进行某种促进和选择。
电极材料的性质是决定电极催化特性的关键因素。电极材料的不同可以使反应速度发生数量级的变化。改变电极材料的性质,既可以通过变换电极基体材料来实现,也可以用有电催化性能的涂层对电极表面进行修饰改性而实现。电极涂层的制备工艺条件对其催化性能有很大的影响。
良好的电催化电极应该具备下列几项性能:
(1)良好的导电性:至少与导电材料(例如石墨)结合后能为电子交换反应提供不引起严重电压降的电子通道,即电极材料的电阻不能太大;
(2)高的催化活性:即能够实现所需要的催化反应,抑制不需要或有害的副反应;
(3)良好的稳定性:能够耐受杂质及中间产物的作用而不致较快地被污染(或中毒)而失活,并且在实现催化反应的电势范围内催化表面不至于因电化学反应而过早失去催化活性;
(4)良好的机械物理性质:即表面层不脱落、不溶解。
催化剂之所以能改变电极反应的速率,是由于催化剂与反应物之间存在的某种相互作用改变了反应进行的途径,降低了反应的活化能。在电催化过程中,催化反应是发生在催化电极/电解液的界面,即反应物分子必须与电催化电极发生相互作用,而相互作用的强弱则主要决定于催化电极表面的结构和组成。
(1)表面材料
电极对催化剂的要求满足:反应表面积要大;有较好的导电能力;吸附选择性强;在使用环境下的长期稳定性;机械性能好;资源丰富且成本低;环境友好。
目前已知电催化电极表面材料主要涉及过渡金属及半导体化合物。
A. 过渡金属:
由于过渡金属的原子结构中有空余的d轨道(一种原子轨道)和未成对的d电子,通过含过渡金属的催化剂与反应物分子的电子接触,这些催化剂空余d轨道上将形成各种特征的吸附键达到分子活化的目的,从而降低了复杂反应的活化能,达到电催化目的,因此,过渡金属及其一些化合物本身具有较好的催化活性 。
B. 半导体化合物:
由于半导体的特殊能带结构,其电极/溶液界面具有一些不同于金属电极的特殊性质,由于产物不易被吸附在电极表面,本身电极表面的氧化速率高于一般电极,因此在电催化问题的研究中,半导体化合物占有特殊重要的位置。
(2) 基础电极
基础电极:也叫电极基质,是指具有一定强度、能够承载催化层的一类物质。一般采用贵金属电极和碳电极。
基础电极无电催化活性,只承担着作为电子载体的功能。
——高的机械强度;
——良好的导电性;
——与电催化组成材料有一定的亲和性。
(3) 载体
基础电极与电催化涂层有时亲和力不够,致使电催化涂层易脱落,严重影响电极寿命。
电催化电极的载体:一类起到将催化物质固定在电极表面,且维持一定强度的一类物质,对电极的催化性能也有很大影响。
常用的载体多采用聚合物膜和一些无机物膜。
载体必须具备良好的导电性及抗电解液腐蚀的性能,其作用可分为两种情况:支持和催化,相应地可以将载体分为两种情况:
(1)支持性载体:仅作为一种惰性支撑物,只参与导电过程,对催化过程不做任何贡献;
——催化物质负载条件不同只会引起活性组分分散度的变化
(2)催化性载体 :载体与负载物存在某种相互作用,这种相互作用的存在修饰了负载物质的电子状态,其结果可能会显著改变负载物质的活性和选择性。同时,载体与负载物之间的结合程度是影响电催化电极性能的重要因素(影响电极的机械强度和稳定性,影响到电极的使用寿命)。
例:铂-三氧化钨Pt-WO3,钛-二氧化锡-二氧化铅Ti-SnO2-PbO2
(3) 电极表面结构
电催化电极的表面微观结构和状态是影响电催化性能的重要因素之一,而电极的制备方法直接影响到电极的表面结构。
目前电催化电极的主要制备方法有热解喷涂法、浸渍法(或涂刷法)、物理气相沉积法(PVD)、化学气相沉积法(CVD)、电沉积法、电化学阳极氧化法,以及溶胶-凝胶法等。
为了增大单位体积的有效反应面积,改善传质,用于三维电极的各种新材料相继问世,如金属碳复合电极,碳纳米管材料等。
总之,无论是提高催化活性还是提高孔积率、改善传质,改进电极表面微观结构都是一个重要手段,因而电极的制备工艺绝对是非常关键的一个环节。
支持电解质:加入到有机废水的电化学处理体系中,可以增强溶液导电性,使有机物的降解反应顺利发生的电解质盐。
基本要求:
(1)当量电导率大:降低电阻,减少能耗;
(2)性质稳定:不参与电化学反应,也不与有机物反应,避免能量损耗,降低电流效率;
(3)无毒无害,且易于去除;
(4)不在电极表面发生特性吸附:避免降低电极的有效反应面积。
例如:对于像Na2SO4这类的惰性电解质,电解过程中不参与反应,只起导电作用,电解效率的高低仅与其浓度有关,而像NaCl等电解质,在电解过程中参与电极反应,Cl-在阳极氧化,进而转变成HClO。
电化学反应器种类繁多、结构复杂、不同的应用领域,所应用的反应器结构和形式均不完全一样,其中,反应器结构和电极结构是影响电化学应用中电流效率的重要因素之一。电化学反应器分为二维反应器和三维反应器,如下表:
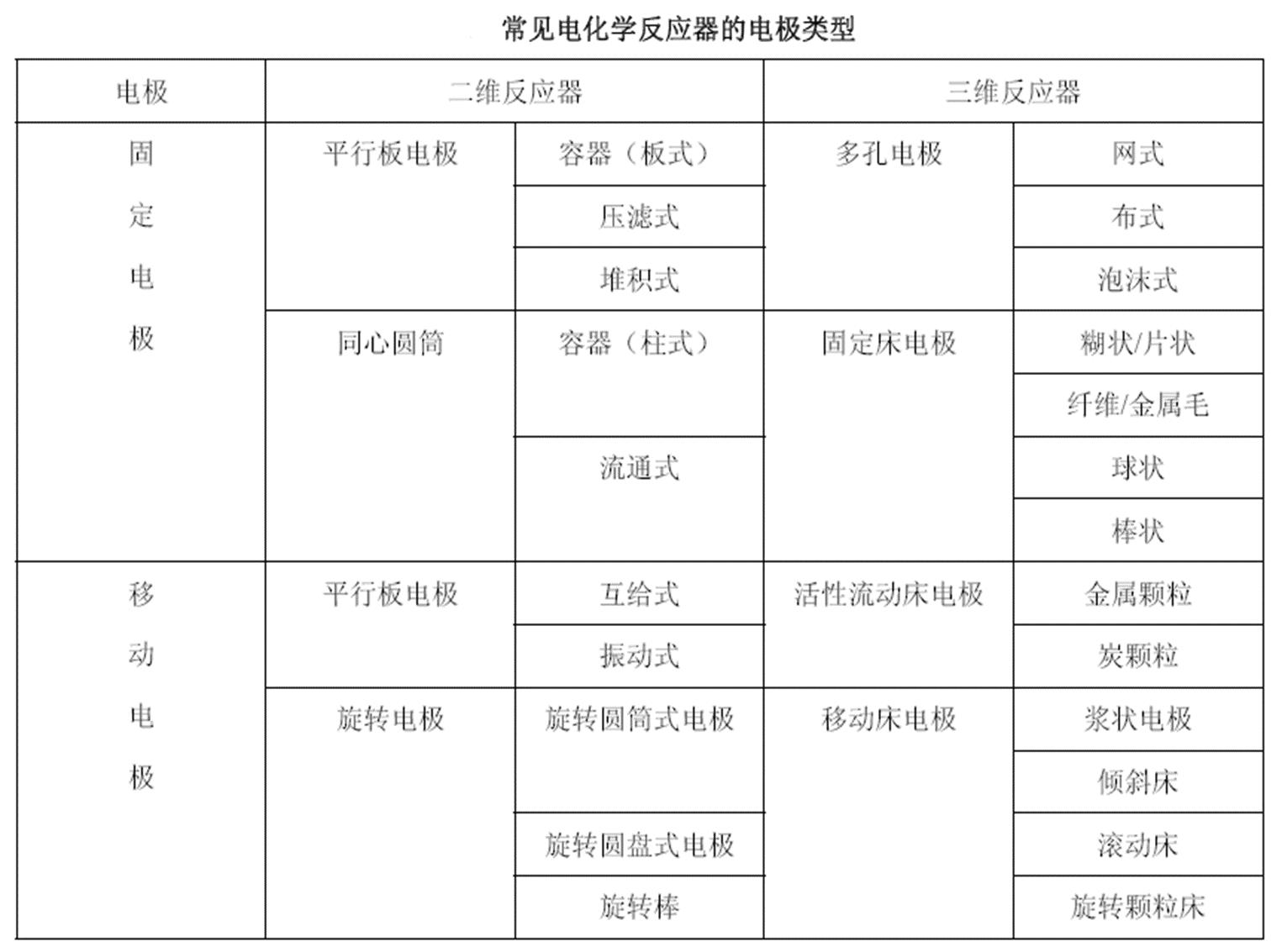
图2-3常见电化学反应器的电极类型
(1)二维电极反应器
传统的电解反应器,只有正负两极,这种反应器的面/体比较小,有效电极面积小,传质问题不能很好解决,在实践中难以有突破性进展,不能满足工业应用的要求。
(2)三维电极反应器
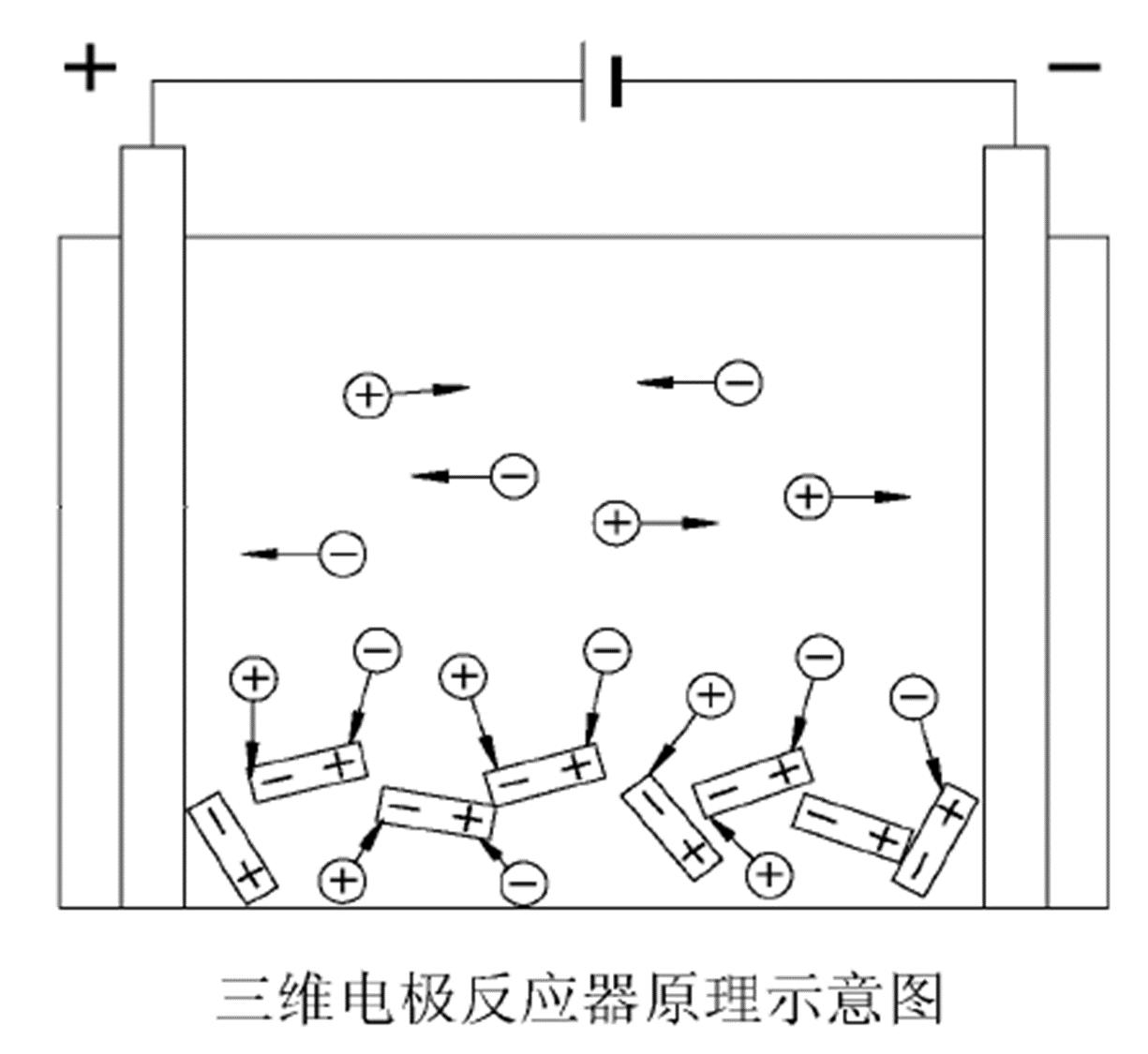
最早于20世纪60年代末期提出的,又称为粒子电极,是一种新型的电极反应器,是在传统二维电解槽电极间填充粒状或其他碎屑状工作电极材料,使装填工作电极材料表面带电,成为新的一极(第三极),在工作电极表面发生电化学反应,从而使有机物降解。
三维电极反应原理:
在阴阳极所产生的电场作用下,电解槽内增加了无数的微电极,能够增加电解槽的面体比,加快对废水有机物的降解。直接氧化是通过阳极直接将有机物氧化降解。间接氧化是指溶液中溶解的氧、外界提供的氧以及阳极电解产生的少量氧在阴极区发生还原反应生成H2O2,进而降解有机物,H2O2在电极上金属催化剂的作用下进一步产生·OH。
三维电极的填料:
在三维电极中,常用的填充材料主要有金属导体、铁氧体、镀有金属的玻璃球或塑料球、石墨以及活性炭等。近年来,用于三维电极的新型碳电极材料相继问世,包括高孔隙率的碳-气凝胶电极,金属-碳复合电极,碳泡沫复合材料以及网状玻碳材料等。另一类新材料是导电陶瓷电极材料。
可应用于金属离子的去除、无机和有机污染物的去除、水体净化、氧化还原剂和其他试剂的循环利用、大气的电化学净化、电絮凝等。电化学过程可以有效地破坏大分子有机物,并降低其毒性,处理后的废水可生化降解性提高。
影响电催化效率的因素主要包括四个方面:电极材料、电解质溶液、废水的理化性质和工艺因素(电化学反应器的结构、电流密度、通电量等)。
(1)电极材料
电极材料选择的好坏,直接影响有机物降解效率的高低(高电势) :
尽量避免竞争副反应(析氧反应);
不同的电极材料可引起电化学反应速度发生数量级上的变化;
研制高电催化活性的电极材料;
为了提高电极的催化活性,一般都对电极进行修饰,其方法有:
A. 在电解液中添加有催化作用的物质;
B. 将电极改为活性高的材料;
C. 对电极材料表面进行修饰。
对电极进行掺杂是改变电极材料组成及其性能的常用的一类方法。
例:掺杂锑(Sb)的二氧化锡(SnO2)电极的导电能力及催化氧化性能都有了很大提高。
——掺杂的SnO2电极对析氧反应具有极高的过电位,较高的电流效率
——卤素和有机卤代物有较强的阻滞作用,减小了处理过程中形成有毒卤代化合物的可能性。
(2)电解质溶液
A. 电解质溶液的浓度
——溶液浓度太低,电流小,降解速率低
——随着电解质溶液浓度的增加,溶液的导电能力增强,电压效率提高。但电解质浓度达到一定浓度后,电压效率的提高趋于平缓,若再加大投入量会增加处理费用。
B. 电解质的种类
Na2S04:惰性电解质,电解过程中不参与反应,只起导电作用,电解效率的高低仅与其浓度有关;
NaCl:在电解过程中参与电极反应,Cl-在阳极氧化,进而转变成HClO,后者是一种强氧化剂,不但可以直接氧化有机物,而且还能阻止有机物(或中间产物)在电极表面的吸附(使电极活性降低)。
缺点:Cl-的加入也可以引起一些副反应,如生成的游离氯或电极上吸附的单原子氯可以与废水中溶解的有机物或其氧化的中间产物反应,生成有毒且更难降解的有机氯化物;Cl-在电极上的吸附影响有机物在电极上的吸附氧化;Cl2的产生也使电流效率有所降低。
(3)废水的理化性质
——同一电极对不同有机物表现出不同的电催化氧化效率;
——废水体系的pH值常常会影响电极的氧化效率,而这种影响不仅与电极的组成有关,也与被氧化物质的种类有关;
——添加支持电解质(如NaCI、 Na2S04)增加废水的电导率,可减少电能消耗,提高处理效率。
(4)工艺因素
——反应器:二维反应器、三维反应器
——电流密度
——电解时间
——溶液传质
不同的有机污染物降解所需的各条件的最佳指标是不同的,有必要深入研究有机物在电极上的氧化历程,开发高效的电极材料,确定最佳的降解条件,提高电解效率,降低水处理费用。
(1)电子转移只在电极及废水组分之间进行,不需要另外添加氧化还原试剂,同时也避免了由另外添加药剂而引起的二次污染问题;
(2)可以通过改变外加电流、电压,随时间调节反应条件,可控制性较强;
(3)反应过程中可能产生的自由基可以无选择地直接与废水中的有机污染物反应,可将其降解为CO2、H2O和简单低分子有机物,没有或很少产生二次污染;
(4)能量效率高,反应条件较温和,电化学过程一般在常温常压下即可进行;
(5)反应器设备及其操作一般比较简单,如果设计合理,费用并不昂贵;
(6)当排污规模较小时,可以进行就地处理;
(7)当废水中含有金属离子时,阴、阳两极可同时起作用(阴极还原金属离子,阳极氧化有机物),使处理效率提高,同时回收再利用有价值的化学品或金属,避免了二次污染;
(8)兼有吸附、絮凝、杀菌作用;
(9)作为一种清洁工艺,设备占地面积小,特别适合于人口拥挤的城市中污水的处理;
(10)既可以单独处理,又可以与其他处理方法相结合,例如作为前处理,可以将难降解有机物或生物毒性污染物转化为可降解物质,从而提高废水的可生物降解性。
(1)电解法处理有机污染物的机理探讨还很不充分,不能对电极的选择、工艺的设计、工艺参数的确立起到具体的理论指导作用;
(2)电流效率仍然很低,经济上不合理。现在研究的电极价格偏高(主要指各种贵金属电极或钛基电极),处理过程耗电量很大,即实用化的电极材料不多,且寿命一般都不长,因此处理的成本比较高,不适合大规模推广,因此,制备出高效的复合型电极是将其工业化应用的前提;
(3)三维电极的引入虽然解决了传质问题,但又引起了床内电流和电压的分布问题,虽然有些理论模型与实验测试取得了一致,但对指导实际应用来说还是不够的;再者,三维电极的电极堵塞也是急需解决的问题之一,设计出高效合理的的反应器,也是将其工业化推广应用所必须解决的问题。
(1)应用前景
A、在电解过程中产生强氧化性的物质,使有机污染物均相或异相地被彻底氧化降解成二氧化碳和水;
B、把生物难降解的有机物通过电化学方法转化为易生物降解的有机小分子或把有毒有机物转变成无毒有机物,主要是通过电解使环状化合物开环,生成易生物降解的脂肪类化合物。
(2)研究方向(目标:工业化应用)
A、研制新型电极材料,以提高电流效率和催化活性,实现有机污染物低成本去除;
B、 深入研究电化学氧化机理,以便针对特定污染物和处理要求设计制造特性电极;
C、改进工艺条件,以减少能量消耗,降低运行成本,提高处理效率;
D、 提高智能化水平,以突出电化学方法易于控制的优点,稳定处理效果,实现自动化运行。
E、工业废水往往成分复杂,采用单一的电化学氧化处理效果往往不够稳定可靠。将电催化氧化技术与其他物理法化学法联合运行,一定条件下可产生协同效应,提高有机物的降解速率,降低处理成本,因此研究组合工艺意义重大。